专家提醒,研发投入大,失败率高,企业切勿跟风乱入
(上接D01版)
PD-1/PD-L1抗体打响市场争夺战
目前,抗癌药中最炙手可热的非PD-1/PD-L1抗体莫属,其广泛的抗癌性和积极的疗效让不少肿瘤患者从中受益。自2014年至今,全世界已有5种PD-1/PD-L1抗体获批上市,包括2种PD-1抗体和3种PD-L1抗体,用于治疗十几种癌症,包括肺癌、肝癌、胃癌、黑色素瘤等。
6月15日,百时美施贵宝的PD-1单抗药物纳武利尤单抗(Opdivo,俗称“O药”)获得国家药监局批准上市,成为第一个在中国上市的PD-1抗体。紧随其后的是默沙东的帕博丽珠单抗(Keytruda,俗称“K药”),于7月25日获批上市。
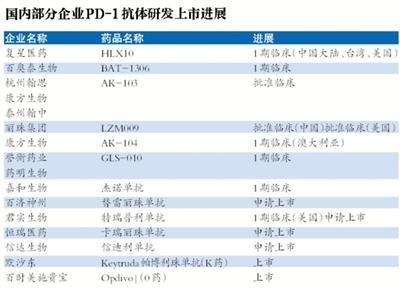
随着中国新药审评审批的加速,PD-1/PD-L1抗体研发和市场打响争夺战。8月31日,百济神州发布公告,其PD-1抗体替雷丽珠单抗的上市申请获得受理,适应症为复发/难治性经典型霍奇金淋巴瘤(R/R cHL)。这是国内第6个申请上市的PD-1/PD-L1抗体。此前,恒瑞医药的卡瑞丽珠单抗、君实生物的特瑞普利单抗、信达生物的信迪利单抗已经提出上市申请。
火石研究院发布的数据显示,截至8月1日,国内已有34个PD-1/PD-L1单抗获药审中心受理(包括已上市的两款产品),涉及28家国内企业,6家境外企业。国内公开登记的PD-1/PD-L1抗体临床试验已有133项,涉及14家国内企业的16个品种,6家国外企业的6个品种;从临床阶段看,III期临床56项,II期临床32项,I期临床35项,其他10项,III期临床占比达42%。
业内人士推测,目前至少有100多家企业涉足PD-1/PD-L1抗体的研发,其中仅有20多种获批临床试验,大部分还处于临床前。
【名词解释】
PD-1和PD-L1
PD-1是程序性死亡受体1,是免疫T细胞表面的一种受体蛋白;PD-L1则是存在于肿瘤细胞表面的一种配体蛋白。这两者一旦结合,会抑制免疫系统,让癌细胞肆无忌惮地生长。
PD-1/PD-L1抗体就是把其中一个通路限制住,不让两者结合,让免疫系统能正常工作,攻击肿瘤细胞。
■ 业内声音
企业入场应先评估自身实力
医药行业创新具有大投入、长周期、高风险的特点,产品从研发到上市需要耗费10 年以上时间,这期间任何决策的偏差、技术上的失误都将影响创新成果。尤其是抗癌药物,研发投入大,成功率却很低。
国家卫生健康委药政司司长于竞进在4月28日的国务院新闻办例行新闻发布会上曾提到,我国已上市抗癌药品138种,2017年总费用约1300亿元。近年来,各方加大抗癌药前期研发投入,但新产品研发成功率不到2%,平均成本超过7亿美元。
“产品战略对企业的未来发展非常重要,现在很多企业头脑发热,盲目跟风。一定要冷静分析自身是否有进入抗肿瘤药研发的资本,否则可能几千万、几亿元都打了水漂。”史立臣指出,医药行业的品类变化非常缓慢,从市场规律而言,只有最先研发成功的前三名能抢占市场优势,大部分企业在这其中并不受益。创新药研发投入巨大,如果企业自身资金不雄厚,主销产品又不是抗肿瘤药,不建议进入这个市场。
另外,政策还存在着可能的变动,会对企业在抗肿瘤药领域布局产生影响。史立臣指出,目前抗肿瘤药物加快进入医保目录,其他药品,如拥有庞大患者群体的心脑血管疾病药物的进入速度并未加快,势必影响到这些药品所占的医保份额。“现在只是因为热点问题把肿瘤药拱起来了,实际上应该让重大疾病相关药物有序地进入医保目录。这个政策我认为未来两三年可能会调整,如果此时不考虑到这个问题而盲目投入,很多企业的研发会陷入被动。”
抗肿瘤药市场进入“战国时代”(1)
发布日期:2019-05-29 来源:网络整理 浏览量:
次
最新新闻
热门新闻